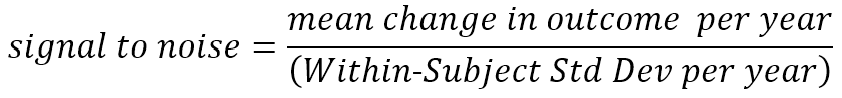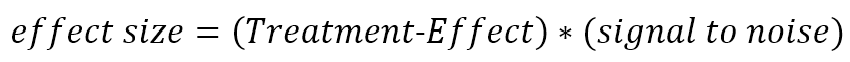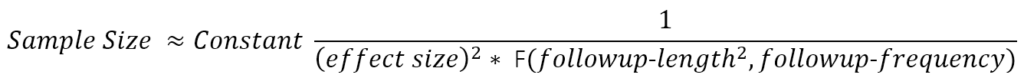Uso de datos observacionales como base del diseño de ensayos clínicos
Modelado de la progresión natural de la enfermedad de posibles resultados de ensayos clínicos.
Introducción
En las últimas dos décadas se han realizado varios estudios observacionales de gran tamaño sobre la progresión de la EH (Biglan et al. 2016, Dorsey et al. 2013, Orth et al. 2011, Paulsen et al. 2014, Tabrizi et al. 2013). El mayor de estos estudios, Enroll-HD (Landwehrmeyer et al. 2017), está en curso y proporciona conjuntos de datos de acceso abierto para los investigadores. El objetivo principal de estos estudios observacionales es proporcionar una mejor comprensión de la historia natural mensurable de la EH, que es necesaria para informar el diseño de ensayos clínicos de terapias candidatas que apuntan a retardar la progresión de la enfermedad. Aquí describimos algunas consideraciones clave con respecto a los datos observacionales de HD y su análisis que son especialmente pertinentes para el diseño de ensayos clínicos.
La historia natural de la progresión de la EH y el diseño de ensayos clínicos.
Un objetivo central del diseño de ensayos clínicos es maximizar las posibilidades de demostrar la eficacia convincente del tratamiento de la manera más eficiente posible, minimizando la exposición a cualquier daño potencial proveniente de un tratamiento no probado, así como los plazos hasta la presentación para la aprobación de un tratamiento eficaz o el abandono de un tratamiento. uno ineficaz. También minimiza los costos financieros y de oportunidad de evaluar un candidato terapéutico, una consideración central cuando la industria decide dónde y cómo invertir recursos.
La eficacia se define como una mejora significativa a lo largo del tiempo en la tasa de progresión de la enfermedad o la tasa de eventos relacionados con la enfermedad en comparación con un grupo de control (a menudo un grupo de placebo) cuya experiencia representa la progresión de la enfermedad cuando todas las influencias potenciales distintas del tratamiento son idénticas. La experiencia del grupo de control representará una combinación de progresión natural de la enfermedad (generalmente dentro del contexto del estándar de tratamiento actual) y posibles modificadores (por ejemplo, efectos placebo) debido a la participación en el ensayo. Generalmente se anticipa que la historia natural será la influencia dominante en el grupo de control, lo que subraya la relevancia y la importancia de los estudios observacionales a partir de los cuales se pueden medir los efectos de estas enfermedades y luego predecirlos para un ensayo clínico futuro.
Aspectos clave del cambio de EH estimados a partir de estudios observacionales
Nos centramos en la tasa de cambio o la frecuencia de aparición de los fenómenos consecuentes de la EH. En términos generales, cuanto más cambia algo dentro del tiempo 'X' sin la terapia, más fácil es saber si la terapia está teniendo efecto. Si un proceso cambia muy lentamente con el tiempo o es muy raro, entonces, independientemente de cuán central pueda ser para la EH, no será una medida práctica para usar como base de un ensayo clínico.
La tasa de cambio de un resultado no es la única propiedad de medición importante. Las medidas que cambian rápidamente en promedio pero que también fluctúan enormemente con mediciones repetidas en el mismo individuo pueden ser menos útiles que otras medidas que cambian más lenta pero constantemente. Esta consistencia del cambio predecible es de importancia central para determinar qué tan grande debe ser un estudio para detectar con confianza un efecto del tratamiento de HD (Diggle et al. 2002, Schobel et al. 2017). El término "relación señal-ruido" es apropiado cuando se hace referencia a este equilibrio entre la tasa de cambio promedio prevista (señal) y la fluctuación impredecible (ruido). Discutiremos este concepto crucial con más detalle a continuación.
También es de gran interés la interrelación entre la progresión de las medidas individuales. Enroll-HD y bases de datos similares proporcionan una fuente de datos especialmente rica para investigar estas relaciones. Se encuentra disponible una amplia variedad de medidas relacionadas con los aspectos motores, cognitivos y psiquiátricos de la enfermedad, así como medidas resumidas del funcionamiento diario. También están disponibles variables demográficas como el nivel educativo, que tienen efectos potencialmente confusos sobre las relaciones aparentes entre enfermedades.
Para el diseño de ensayos clínicos, las interrelaciones de otras medidas con aquellas que resumen el funcionamiento diario, como la escala UHDRS de Capacidad Funcional Total (TFC), son especialmente importantes. Los reguladores deben estar convencidos de que la vida de un paciente es significativamente mejor si un tratamiento mejora el resultado primario del ensayo. Sin embargo, los resultados que miden directamente "mejor", como el CFT, pueden no ser las medidas que cambian de manera más rápida y predecible. Si hay otras medidas o combinaciones de medidas para las cuales el cambio es más fácilmente detectable, un requisito adicional es que esas medidas deben tener al menos una fuerte relación empírica con medidas como el TFC que tienen un significado clínico inherente. Cuando existe una relación empírica fuerte, eventualmente debemos mostrar evidencia de que este vínculo entre las medidas es causal y no simplemente una correlación (Temple 1999, Burzykowski et al., 2005, Administración de Alimentos y Medicamentos de EE. UU. 2018). ¿La mejora en la medida alternativa se traducirá necesariamente en una mejora clínicamente significativa?
Los estudios observacionales nos permiten evaluar las relaciones empíricas entre medidas y es tentador imputar nociones de causa y efecto. Sin embargo, debemos advertir que la cuestión de la causalidad es difícil de responder sin evidencia experimental directa (p. ej., investigación biológica o datos de ensayos clínicos previos). Los analistas de datos observacionales deben ser conscientes de que existen varias técnicas estadísticas que intentan abordar la causalidad dentro de los datos observacionales, y que pueden ser útiles para refinar qué relaciones empíricas son plausiblemente causales. Sin embargo, estas técnicas también requieren que aceptemos varios supuestos sólidos (y a menudo no comprobables) sobre la naturaleza de los datos. Confiar en tales supuestos puede resultar inaceptable en un contexto regulatorio.
Medidas de pronóstico y predicción del cambio.
En igualdad de condiciones, los efectos del tratamiento se detectan más fácilmente con menos participantes y en un tiempo más corto entre aquellos que muestran el cambio más rápido y consistente en la medida de resultado (Langbehn y Hersch 2020). De manera similar, si el resultado es un evento distinto, como la pérdida de la capacidad de vivir de forma independiente, el efecto del tratamiento se detecta más fácilmente entre aquellos que tienen la mayor probabilidad de experimentar el evento durante la duración de un ensayo clínico. Los conjuntos de datos de observación como Enroll-HD no solo permiten estudiar el cambio de la EH a lo largo del tiempo, sino también investigar las características iniciales que ayudan a predecir cambios futuros (pronóstico). En ensayos futuros, estas medidas de referencia podrían usarse como parte de los criterios de selección de participantes para que el ensayo se "enriquezca" con aquellos cuya enfermedad progresará más rápidamente.
Sin embargo, nunca debemos asumir acríticamente que todas las demás cosas son iguales. La ventaja potencial del enriquecimiento de los ensayos a menudo se calcula bajo el supuesto de que la respuesta al tratamiento no está relacionada con la agresividad del pronóstico. Es posible que eso no sea cierto y, a menudo, puede ser más realista considerar una variedad de posibles relaciones entre el pronóstico y la respuesta al tratamiento. Para llevar esto un paso más allá, en algunos casos podemos decidir que se deben utilizar los datos de pronóstico iniciales para definir una ventana terapéutica adecuada para la terapia propuesta, excluyendo en el cribado a aquellos para quienes los cambios de la enfermedad probablemente sean demasiado agresivos, así como para aquellos en quienes será demasiado lento.
Incluso si no se utiliza el enriquecimiento del cribado, en muchos diseños de ensayos el poder para detectar un efecto del tratamiento puede aumentar notablemente mediante el control estadístico de las características pronósticas iniciales en el análisis de los datos finales del ensayo (dicho control estadístico debe ser una característica preespecificada del análisis definitivo). análisis de ensayos clínicos.) Las características iniciales pueden explicar (predecir) parte del “ruido” en los datos de resultados, aumentando efectivamente la relación señal-ruido relevante para probar el efecto del tratamiento (Julious 2010). La ventaja potencial de dicho control estadístico puede estimarse a partir de datos longitudinales observacionales, por ejemplo, investigando la reducción de la variación aparentemente aleatoria en un resultado cuando se utiliza un factor pronóstico como covariable en un modelo longitudinal de progresión no tratada.
Modelar un subconjunto apropiado de datos de observación.
Para que los datos observacionales sirvan de base para el diseño del ensayo clínico, se debe elegir el subconjunto relevante de participantes para el análisis. Este principio de relevancia es obvio en algunos aspectos: si vamos a modelar un ensayo dirigido a las primeras etapas de la EH diagnosticada, entonces queremos limitar nuestros análisis observacionales a los participantes en esa etapa temprana de la enfermedad. Sin embargo, hay aspectos más sutiles de la relevancia que a veces se pasan por alto. Por ejemplo, Enroll-HD contiene datos de seguimiento longitudinal de algunos participantes durante mucho más tiempo que la duración realista de un ensayo clínico. Utilizando sus datos de referencia, puede ser apropiado incluir a dichos participantes en un modelo de prueba. Sin embargo, después de muchos años, estos participantes a menudo habrán superado la etapa relevante de la enfermedad. Por lo tanto, es posible que deseemos limitar los datos longitudinales que se analizan solo a los primeros años de seguimiento (Langbehn y Hersch 2020). (De manera similar, los participantes con un seguimiento prolongado pueden haber evolucionado al grupo de estudio objetivo, incluso cuando habrían sido excluidos con la selección de solo sus datos iniciales. Una serie de observaciones posteriores de dichos participantes podría ser una contribución válida para los datos que se estén analizado.)
Un (poquito) de matemáticas.
Podemos agudizar nuestra apreciación de la relevancia de los datos observacionales para el diseño de ensayos clínicos si prestamos brevemente nuestra atención a una fórmula matemática clave que describe las relaciones aproximadas entre el tamaño de la muestra, el tiempo de seguimiento, el efecto del tratamiento y la tasa de resultados no tratados. medida de progresión. El objetivo es apreciar que el tamaño de la muestra varía como el valor al cuadrado de importantes características de medición, dos de las cuales pueden estimarse a partir de datos de estudios observacionales.
Anteriormente, apelamos a una comprensión intuitiva del término relación señal-ruido. Ahora definimos con mayor precisión lo que queremos decir con el término. Aquí nos referimos al cambio por año, pero la definición se puede aplicar a cualquier unidad apropiada de tiempo de seguimiento.
La señal que deseamos detectar (y esperamos cambiar con una terapia) es la cantidad media de cambio (verdadero) que ocurre a lo largo del tiempo. El ruido, en el denominador, refleja la desviación impredecible alrededor de la tasa de cambio media de cada participante; este ruido a veces se denomina error de medición, pero ese término puede ser engañoso (en este contexto, el ruido también incluye desviaciones reales a corto plazo de la tendencia media a largo plazo, por ejemplo, las señales del motor de un HDGEC varían un poco de un día a otro alrededor del mundo). su media a corto plazo; la variación en las puntuaciones motoras UHDRS registradas que reflejan perfectamente esta variación real alrededor del aumento de la puntuación motora promedio, no obstante, cuenta como ruido para nuestros propósitos.) En ausencia de datos sustanciales de ensayos clínicos previos, esta relación señal-ruido se estima a partir de datos de observación longitudinal obtenidos en estudios como el Enroll-HD. (Se calcula más comúnmente utilizando las estimaciones de efectos fijos y componentes de varianza de un modelo longitudinal de efectos mixtos de dichos datos).
El factor por el cual un tratamiento cambia la tasa media de disminución se refleja en el tamaño del efecto del tratamiento.
Por ejemplo, si un grupo de tratamiento experimentó una disminución media del CFT de 0,6 puntos por año y la disminución media del grupo de control fue de 1,2 puntos por año, entonces el efecto del tratamiento sería 0,6/1,2 = 0,5. La traducción del efecto del tratamiento al tamaño del efecto transmite la magnitud del efecto del tratamiento en unidades de desviaciones estándar dentro de los participantes. Esta es la unidad de medida que determina el tamaño de la muestra para un ensayo clínico. En el ejemplo anterior, supongamos además que la desviación estándar anual del cambio de CFT dentro de los individuos es de 0,8 puntos por año. La relación señal/ruido (sin tratar) es entonces 1,2/0,8 = 1,5. El tamaño del efecto del tratamiento es 0,5 * 1,5 = 0,75.
Considere un ensayo aleatorio de dos brazos que compare el efecto del tratamiento versus el placebo. El resultado del ensayo es el cambio inducido por el tratamiento en la tasa de progresión de la medida de resultado. La fórmula del tamaño aproximado de la muestra tiene la siguiente forma:
La función F(.) en el denominador proporciona un valor que aumenta aproximadamente con el número y el espaciamiento de las visitas de seguimiento en las que se evalúa el resultado y, más importante aún, con el cuadrado de la duración total del seguimiento (Diggle et al. otros 2002). (F(.) es la suma de los cuadrados de los tiempos de visita ajustados a la media). Esta fórmula es aproximada pero ilustra relaciones que siguen siendo fundamentales en cálculos más detallados que reflejan mejor los detalles realistas de los ensayos (Julious 2010) (p. ej., efectos placebo, caída tasas de salida, múltiples brazos de prueba y diseños adaptables al análisis intermedio). Los diseñadores del ensayo definen la duración y la frecuencia del seguimiento. El efecto del tratamiento clínicamente significativo que uno espera detectar es una cuestión de conjeturas (con suerte, bien razonadas). Esto deja la relación señal-ruido de la medida de resultado como la cantidad crítica que se estimará a partir de datos históricos. Los datos recopilados en estudios observacionales longitudinales diseñados prospectivamente serán a menudo los más adecuados para derivar estas estimaciones.
Nuestro caché cada vez mayor de dichos datos, recopilados de estudios como el Enroll-HD, hace que la EH sea una de las enfermedades cerebrales mejor documentadas. Con el tiempo, la experiencia prospectiva en ensayos de HD permitirá estimar parámetros secundarios importantes, como los efectos placebo y el sesgo inducido por las expectativas de los evaluadores. La mayoría de esos ensayos aún no se han diseñado, y esos diseños dependerán crucialmente de los datos de observación existentes, como los que se analizan aquí.
Referencias
Biglan KM, Shoulson I, Kieburtz K, et al. Asociaciones clínico-genéticas en el estudio observacional prospectivo de Huntington en riesgo (PHAROS): implicaciones para los ensayos clínicos. JAMA Neurol 2016;73(1):102-110.
Burzykowski T, Molenberghs G, Buyse M. La evaluación de criterios de valoración sustitutos. Springer, Nueva York. 2005.
Diggle P, Heagerty P, Lian K, Zeger S Análisis de datos longitudinales, segunda edición. Prensa de la Universidad de Oxford. Oxford Reino Unido. 2002
Dorsey ER, Beck CA, Darwin K, Nichols P, Brocht AF, Biglan KM, Shoulson I; Investigadores del Grupo de Estudio Huntington COHORT. Historia natural de la enfermedad de Huntington. JAMA Neurol. 2013 diciembre;70(12):1520-30. doi: 10.1001/jamaneurol.2013.4408.
Julious SA. Tamaños de muestra para ensayos clínicos. Prensa CRC. Boca Ratón, Florida. 2010.
Landwehrmeyer GB, Fitzer-Attas CJ, Giuliano JD, Gonçalves N, Anderson KE, Cardoso F, Ferreira JJ, Mestre TA, Stout JC, Sampaio C. Análisis de datos de Enroll-HD, una plataforma global de investigación clínica para la enfermedad de Huntington. Práctica clínica de trastornos de movimiento. 22 de junio de 2016;4(2):212-224. doi: 10.1002/mdc3.12388. eCollection 2017 marzo-abril.